Vezi și alte cazuri
Uneori ne putem uita și după zebre..în pancreas!
Pacientă în vârstă de 66 de ani, nefrectomizată în urmă cu 16 ani pentru tumoră Grawitz, cunoscută cu toleranţă alterată la glucoză se prezintă pentru investigarea unei leziuni pancreatice descoperită incidental, fiind asimptomatică.
Clinic: asimptomatică.
Biologic: valori izolat crescute ale GGT, dislipidemie, sindrom inflamator (VSH x 3 N); CRP, markeri tumorali (CEA, CA 19-9), hemogramă- în limite normale.
CT abdomino-pelvin cu substanță de contrast a decelat în regiunea cefalică pancreatică, în vecinatatea venei mezenterice superioare, fără efect compresiv asupra acesteia, o formaţiune net conturată izodensă nativ, cu priză intensă de contrast, cu discret washout în faza venoasă şi tardivă. Fără recidivă tumorală la nivelul lojei renale drepte post nefrectomie, fără alte semne de boala metastatică
Se dozează cromogranina A, polipeptidul pancreatic si 5HIAA – în limite normale.
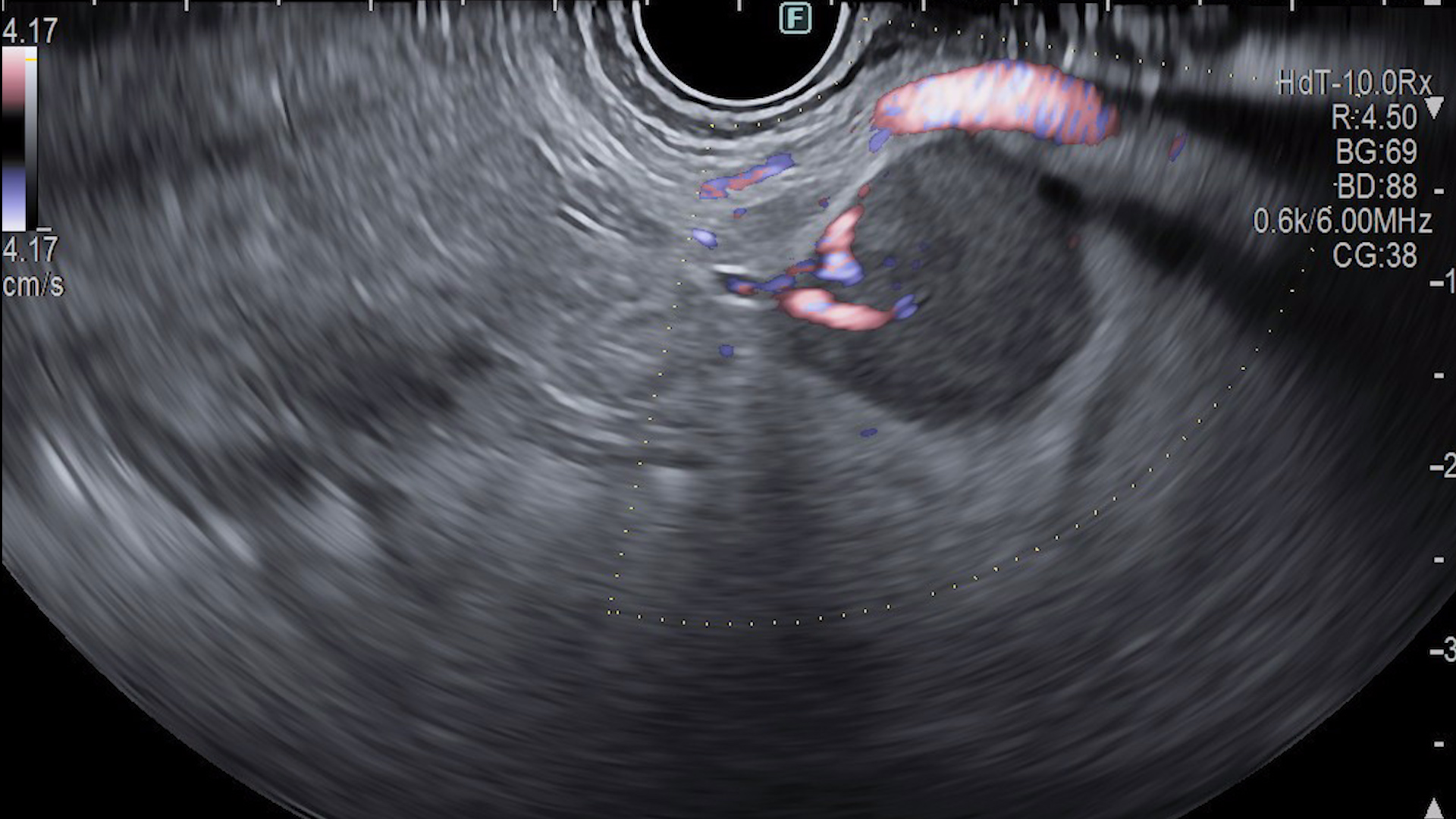
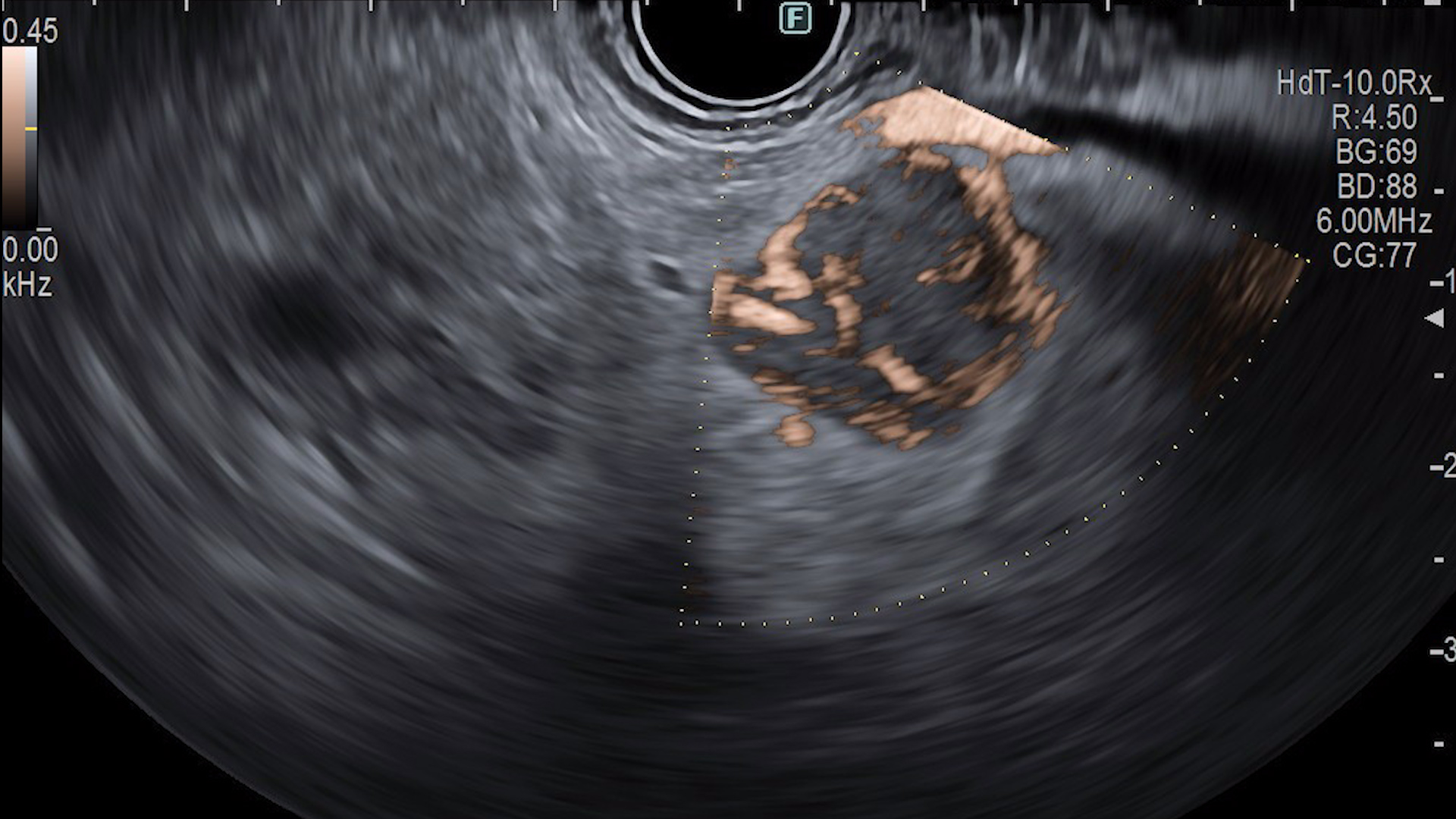
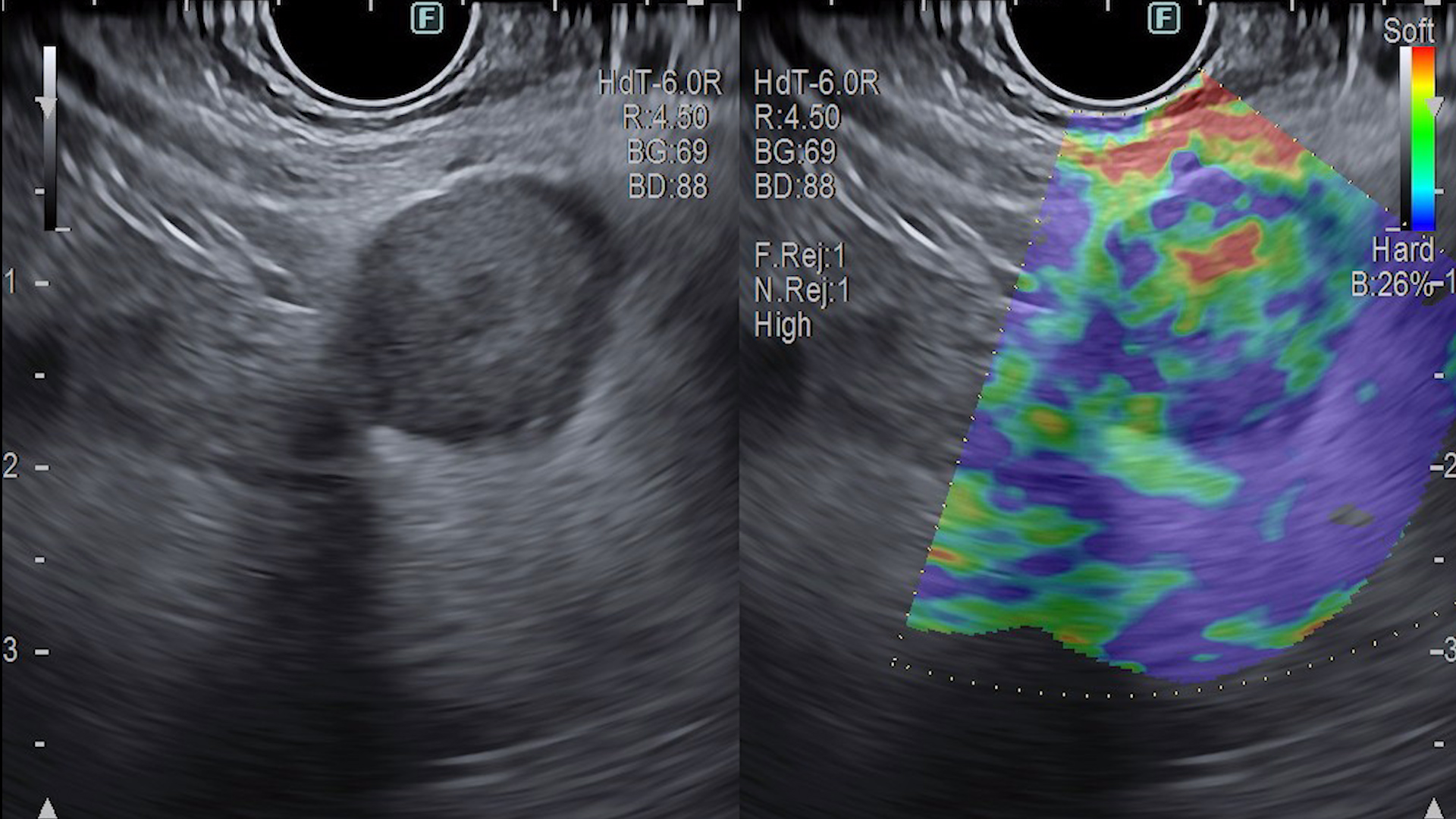
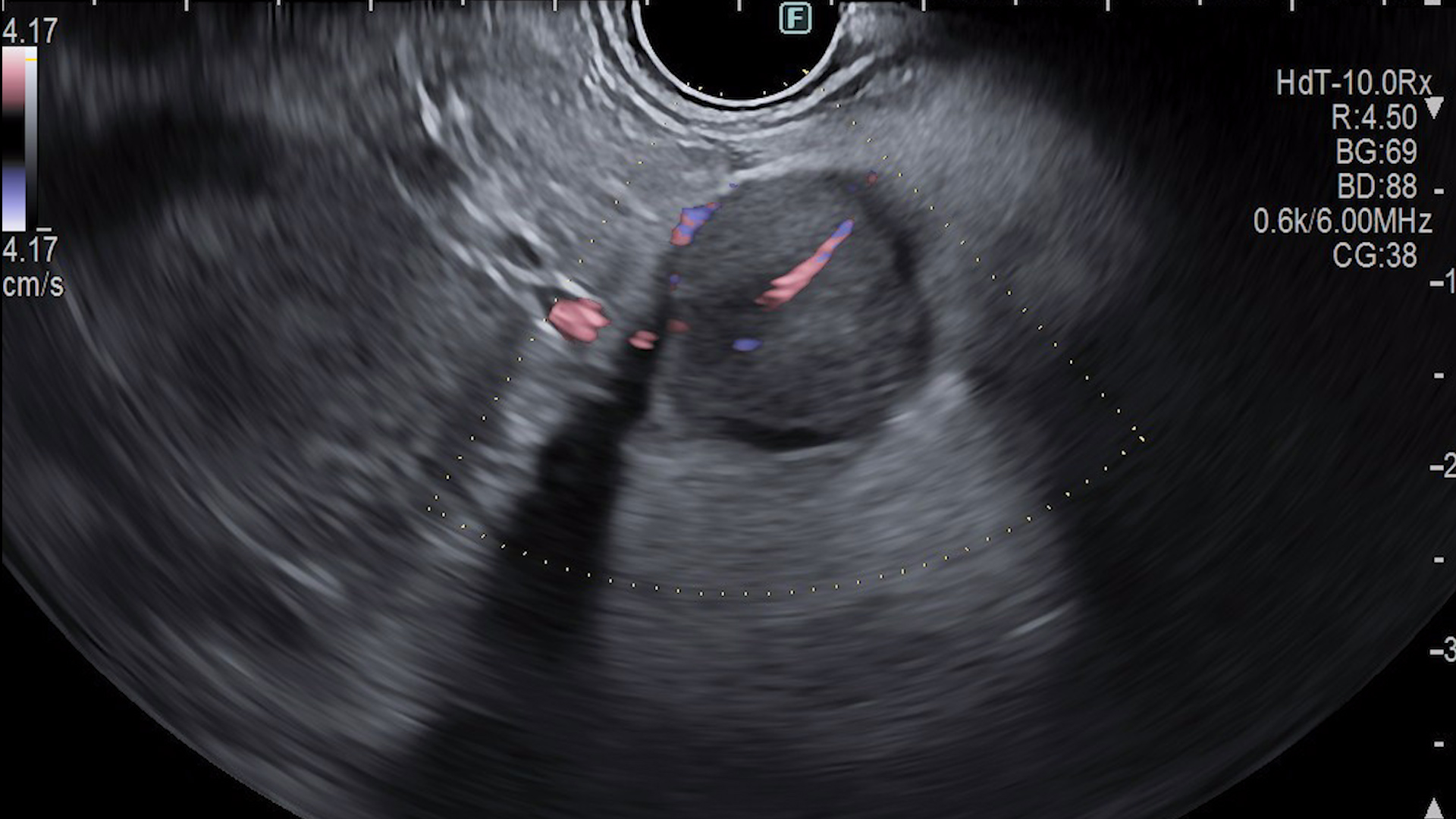
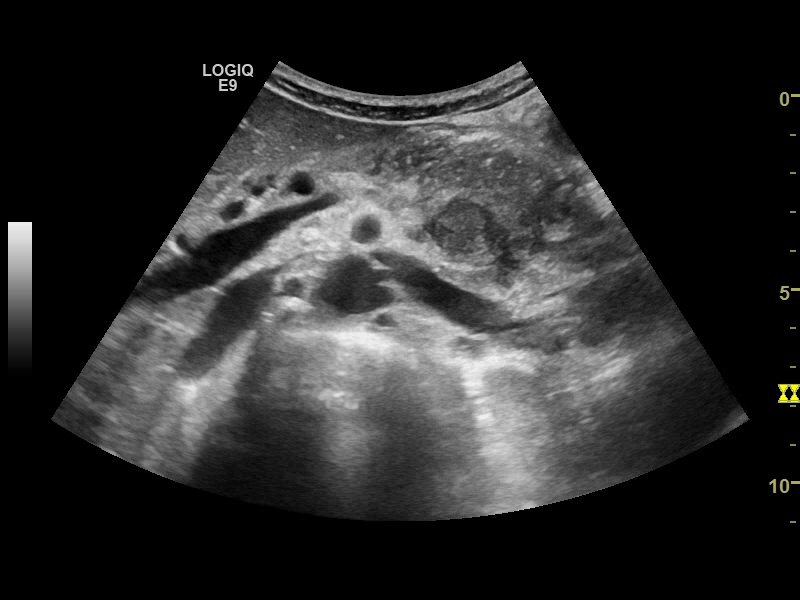
Ecoendoscopic: formaţiune cefalopancreatică hipoecogenă, relativ omogenă, bine delimitată, cu margini regulate, vascularizaţie intens prezentă predominant periferică cu aspect de basket pattern la examinarea Doppler, cu vas nutritiv prezent. Între formaţiune şi structurile învecinate exista plan de clivaj. Aspect elastografic mixt cu valori crescute.
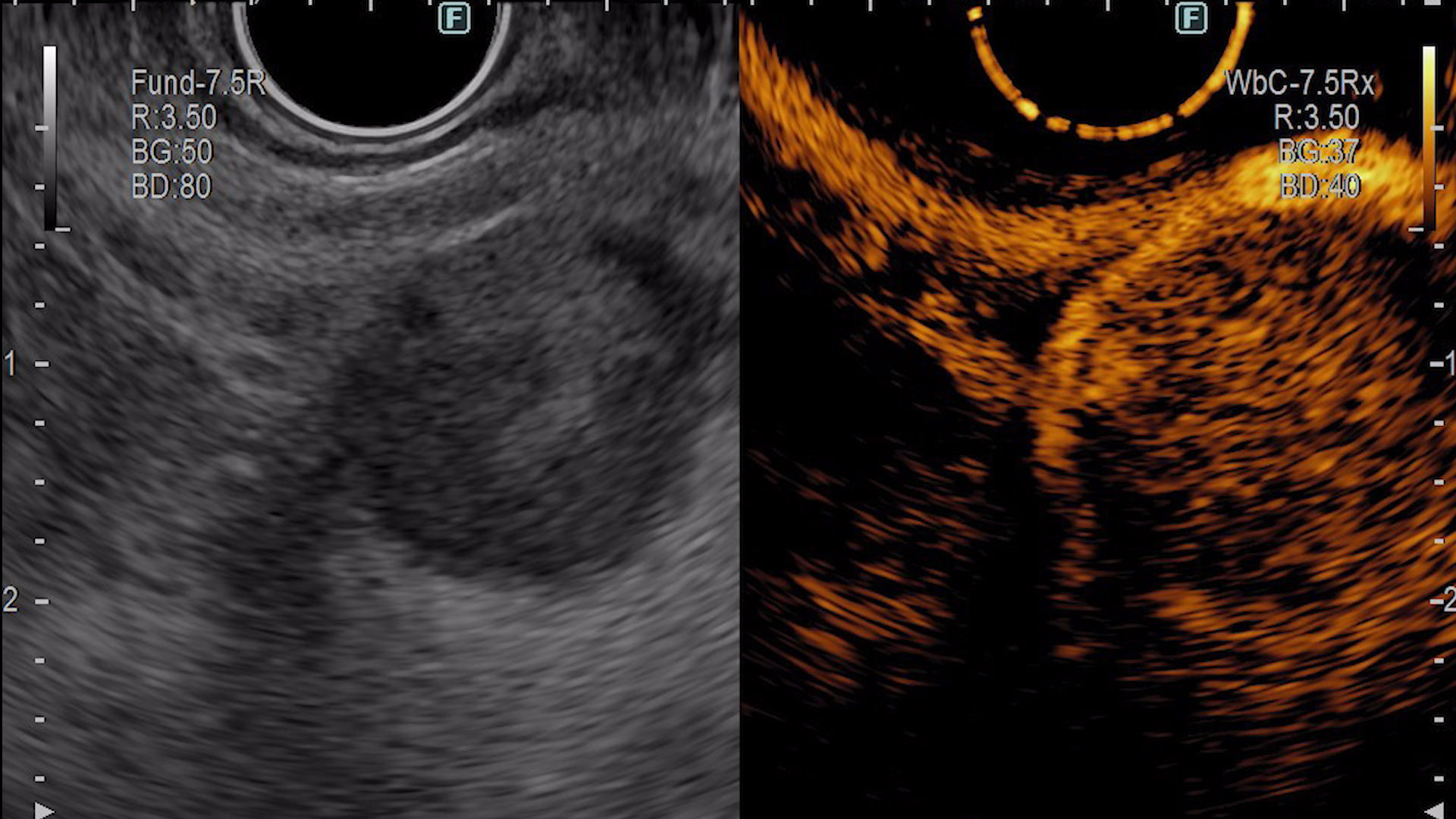
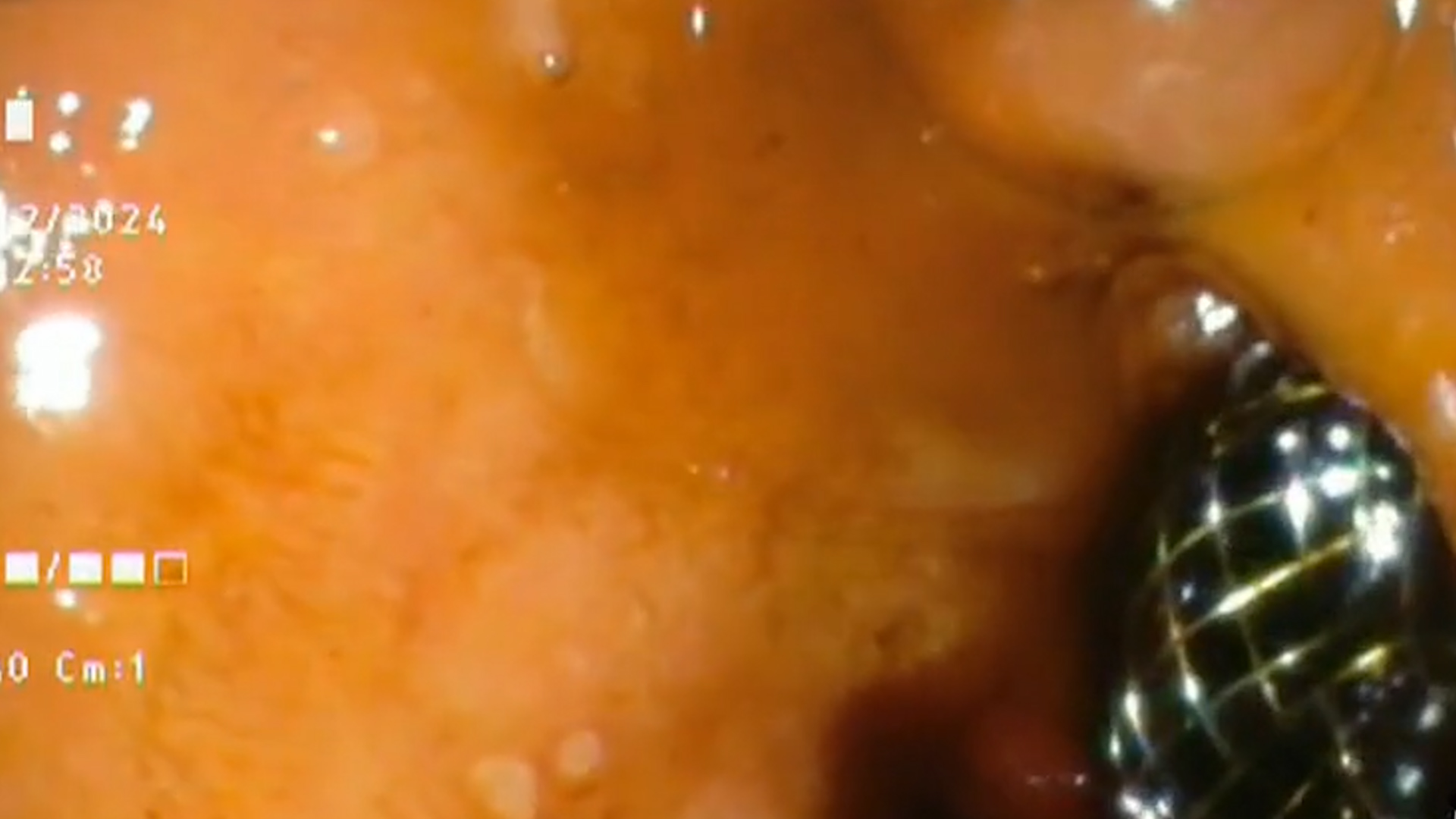
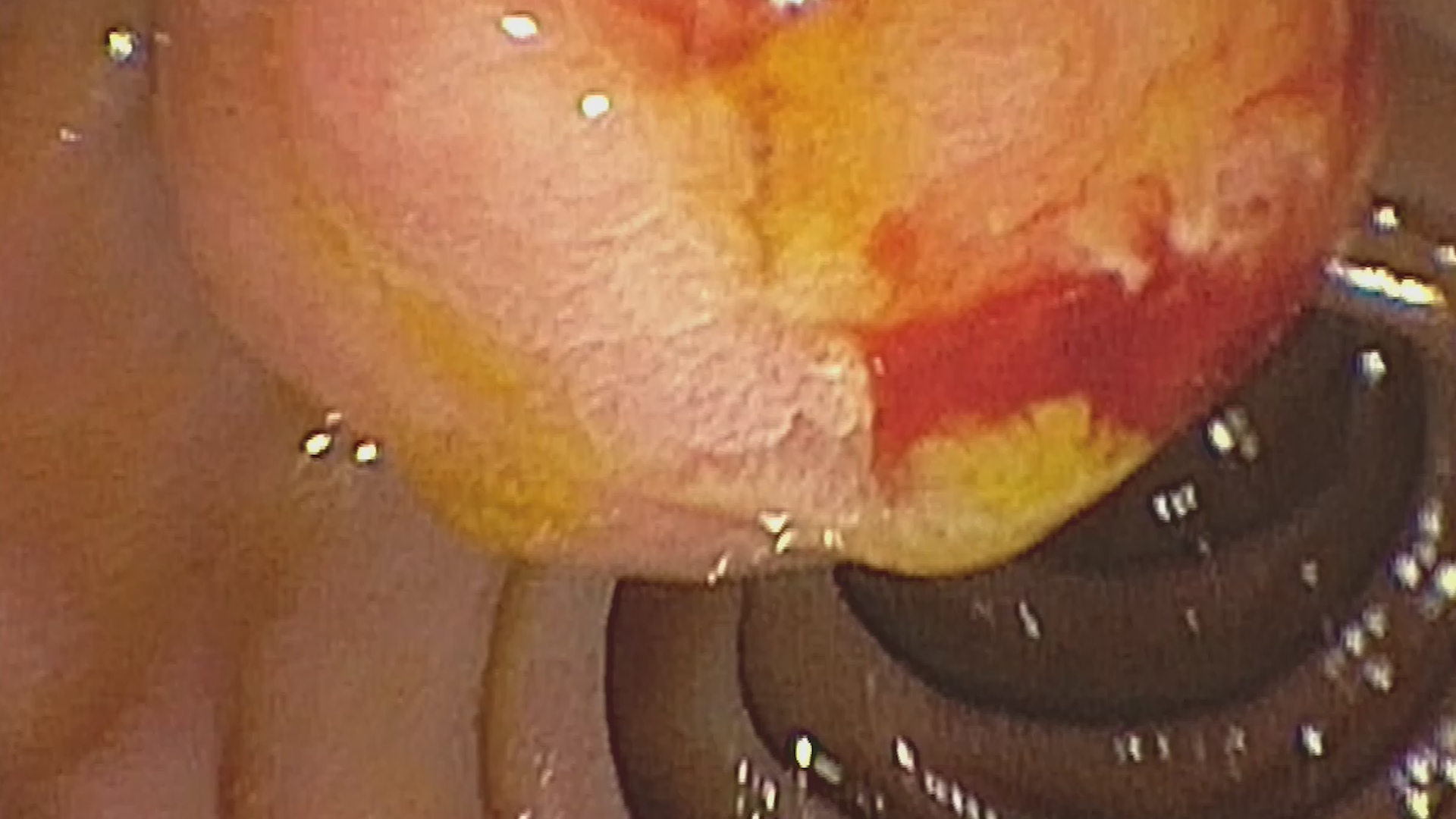
La administrarea substanţei de contrast, în faza arterială, formaţiunea este hipercaptantă, cu contrast predominant periferic dar şi central, cu fenomen washout relativ lent în fază venoasă. Aspectul este sugestiv pentru determinare secundară pancreatică. Se prelevează probe bioptice (FNB) pentru analiză histopatologică ce au clasificat formaţiunea ca fiind determinare secundară pancreatică de la un carcinom renal cu celule clare.
Determinare secundară pancreatică de la un carcinom renal cu celule clare.
Tumorile pancreatice pot fi clasificate în: tumori pancreatice primitive şi determinări secundare (în special întâlnite în cancerul pulmonar, mamar, renal, melanom, neoplasmele gastrointestinale). Metastazele pancreatice sunt entităţi rar întâlnite în practica medicală (1). Examinarea CT este utilă pentru evaluarea formaţiunilor pancreatice având limitele sale, formaţiunile cu dimensiuni foarte mici putând trece neobservate. Examinarea IRM are sensibilitate şi specificitate mai mare faţă de examinările CT, putând detecta formaţiuni pancreatice de dimensiuni mai mici (2).
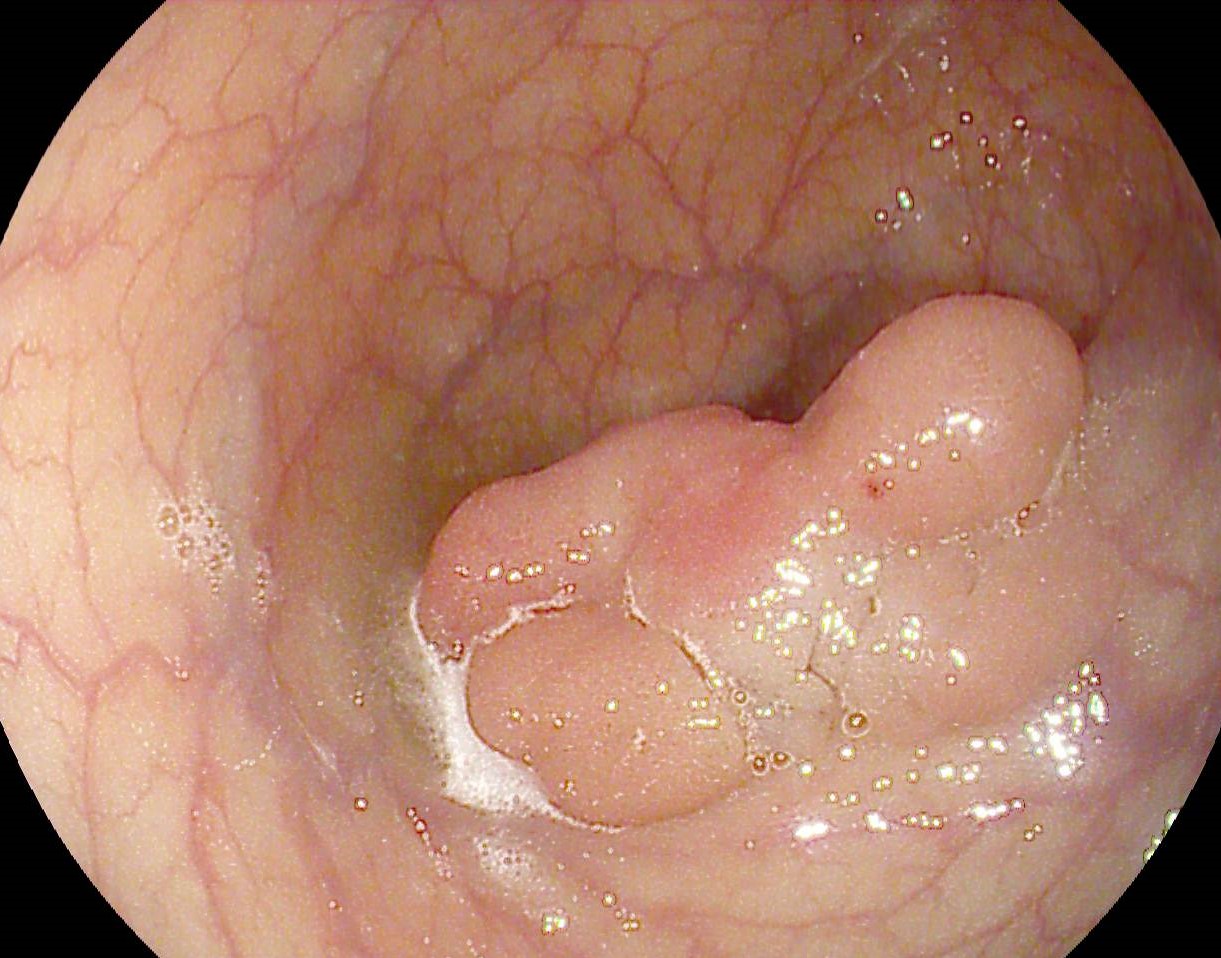
Ecoendoscopia este capabilă să detecteze leziuni mai mici de 2 cm, leziuni care pot rămâne neobservate la evaluările imagistice CT/IRM şi oferă posibilitatea prelevării de biopsii FNA pentru obţinerea unui diagnostic histopatologic de certitudine. Aspectul ecoendoscopic poate orienta diagnosticul. Adenocarcinomul este adesea hipoecogen, slab delimitat, cu sau fără alte criterii de malignitate precum invazia în structurile învecinate şi creşterea în dimensiune a ganglionilor limfatici din proximitate. Tumorile neuroendocrine sunt hipoecogene, cu margini bine delimitate de tesuturile din jur, bine vascularizate. Cel mai frecvent, formatiunile benigne pancreatice apar heterogene cu calcificări. Determinările secundare pancreatice sunt în general bine delimitate, aspectul acestora variază în funcţie de tumora de origine (Fig. 1, 2). (3-5)
Pentru creşterea acurateţei diagnosticului diferenţial al leziunilor pancreatice se poate efectua EUS cu administrarea de substanță de contrast, ceea ce permite evaluarea perfuziei şi patternului de captare al leziunii faţă de țesutul din jur. Astfel, adenocarcinomul este descris ca fiind hipocaptant, NET sunt hipercaptante, iar leziunile benigne izocaptante. Determinarile secundare pancreatice captează substanța de contrast diferit, în funcție de tumora de origine: metastazele neoplasmelor colonice, de sân, de plămân sunt descrise ca fiind hipocaptante, iar cele renale, melanoame și limfoame sunt hipercaptante (Fig. 3). Astfel, EUS își are utilitatea în diagnosticul leziunilor pancreatice, în special pentru formațiunile de mici dimensiuni, iar CEUS în diagnosticul diferențial al acestora. (2, 4). Elastografia EUS poate fi de asemenea folosită pentru creşterea acurateţei diagnostice, ţesutul tumoral având o consistenţă dură, elasticitate mai scăzută în comparaţie cu ţesuturile normale sau fibroase (Fig. 4) (3)
În concluzie, cazul prezentat evidențiază importanța investigațiilor precise și a tehnologiilor avansate de imagistică în diagnosticarea leziunilor pancreatice, în special a determinărilor secundare. Ecoendoscopia cu administrare de substanță de contrast și biopsia ghidată ecoendoscopic (Fig. 5) au jucat un rol crucial în stabilirea diagnosticului corect în acest caz. Continuarea monitorizării și evaluării atente a evoluției pacientului este esențială pentru planificarea unui tratament adecvat și pentru gestionarea optimă a cazului.
- Pancreatic tumors imaging: An update. Int J Surg. 2016 Apr;28 Suppl 1:S142-55. doi: 10.1016/j.ijsu.2015.12.053. Epub 2016 Jan 9. PMID: 26777740. Scialpi M, Reginelli A, D’Andrea A, Gravante S, Falcone G, Baccari P, Manganaro L, Palumbo B, Cappabianca S.
- Imaging of the Pancreas. Ming-ming Xu, MD, Amrita Sethi, MD*. 2016.
- Endoscopic ultrasound of pancreatic tumors. Wangermez, M. s.l. : Elsevier, 2016.
- Yamashita Y, Kitano M. Endoscopic ultrasonography for pancreatic solid lesions. J Med Ultrason (2001). 2020 Jul and 31385143., 47(3):377-387. doi: 10.1007/s10396-019-00959-x. Epub 2019 Aug 6. PMID:.
- Sakamoto H, Kitano M, Kamata K, El-Masry M, Kudo M. Diagnosis of pancreatic tumors by endoscopic ultrasonography. World J Radiol. 2010 Apr 28;2(4):122-34. doi: 10.4329/wjr.v2.i4.122. PMID: 21160578; PMCID: PMC2999320.