Vezi și alte cazuri
Gastrinom MEN1
Bărbat de 43 de ani cu scaune multiple/zi (până la 20) și scădere în greutate, cu explorări imagistice în limite normale (endoscopie digestivă superioară și inferioară, respective CT și RM!), cu tratamente repetate pentru sindrom de intestin iritabil în ultimii 2 ani (Ibutin, Debridat, Normix, Meteospasmyl, nenumarate pre- și probiotice).
Dureri în etajul abdominal superior, scaune multiple/zi (până la 20) și scădere în greutate (> 20kg).
Explorări biologice: cromogranină A (780 ng/mL – Jan 2020; 1140 ng/mL – Feb 2020; 1380 ng/mL – Mar 2020) și gastrină (1200 pg/L) crescute, respectiv serotonină, elastază, 5HIIA normale.
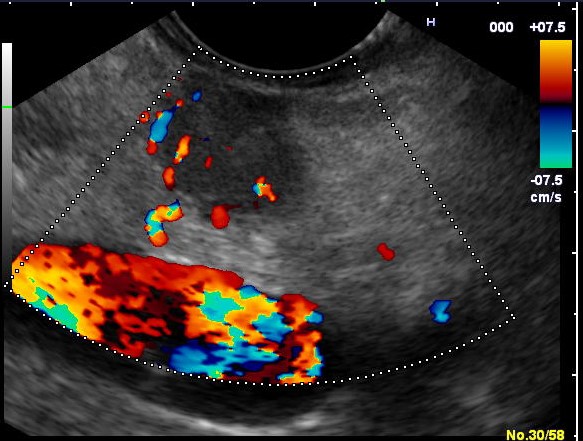
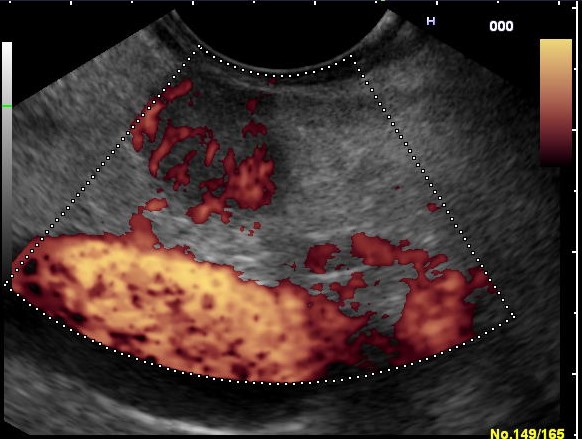
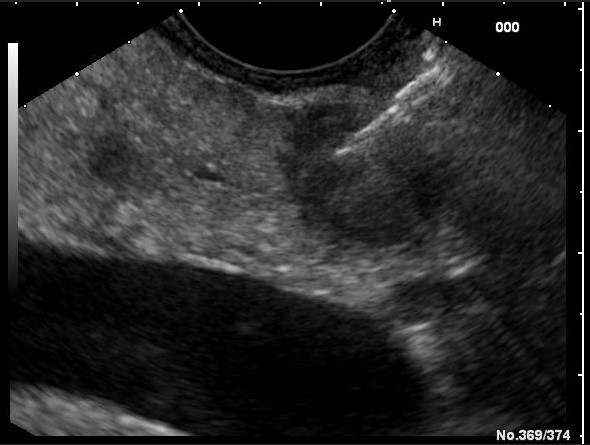
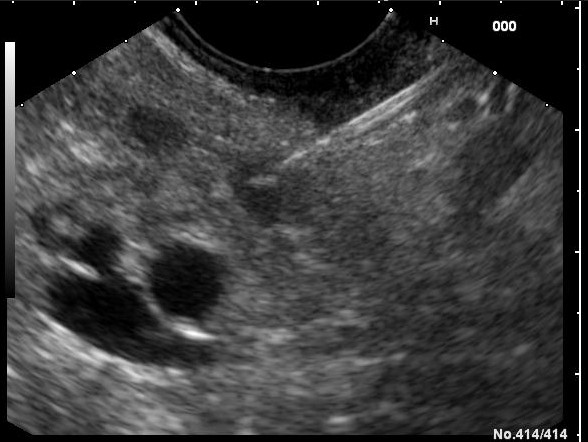
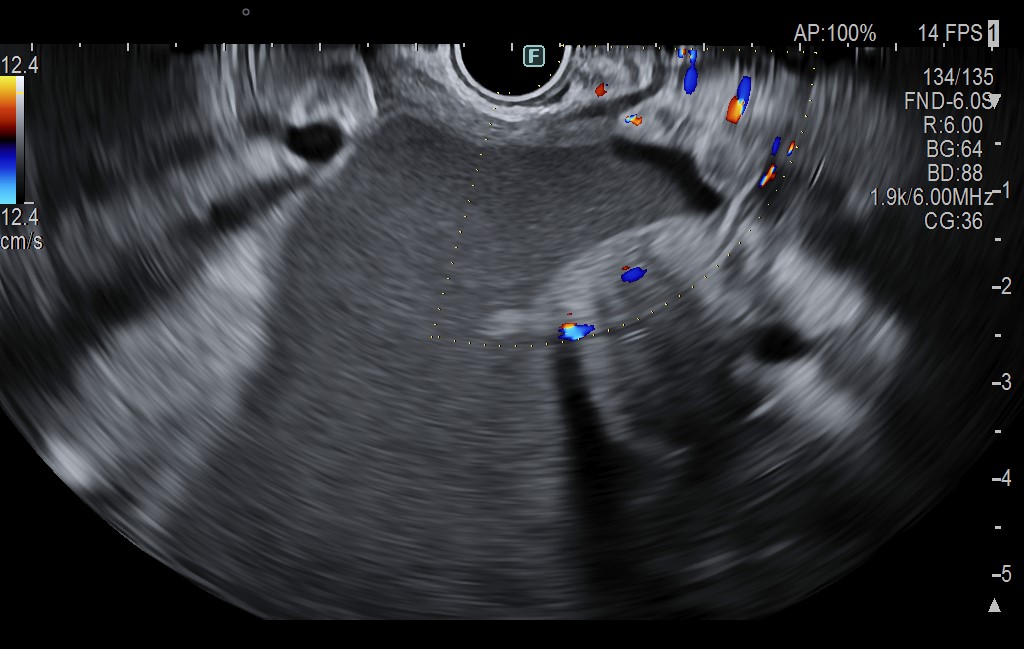
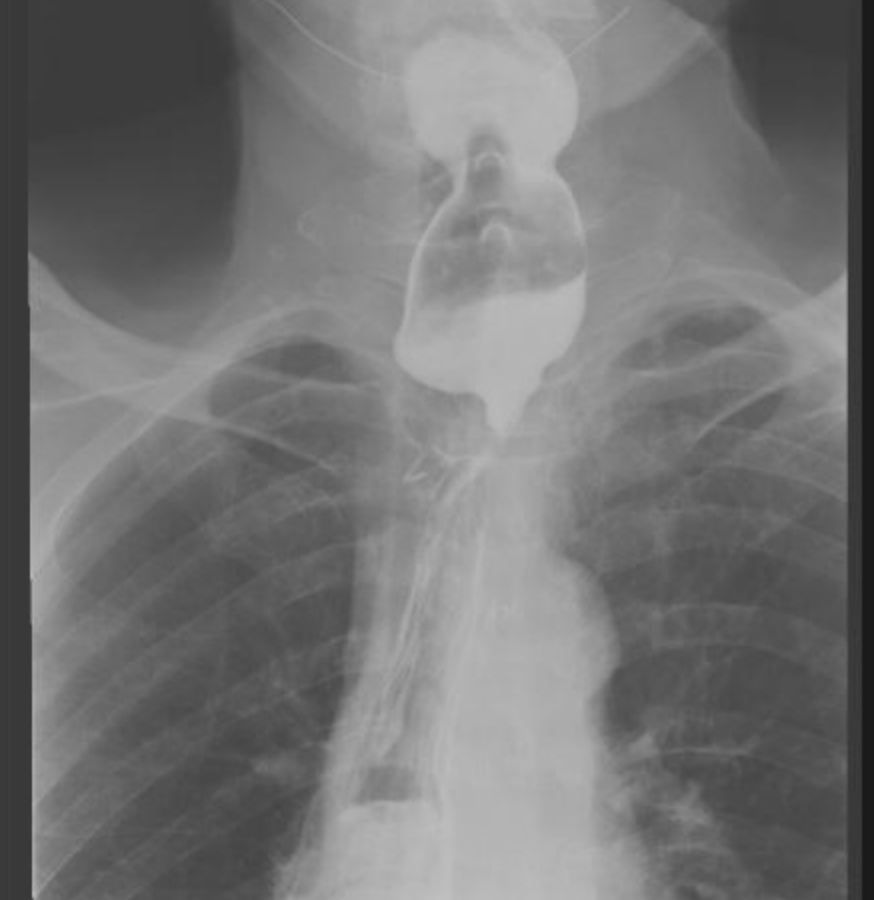
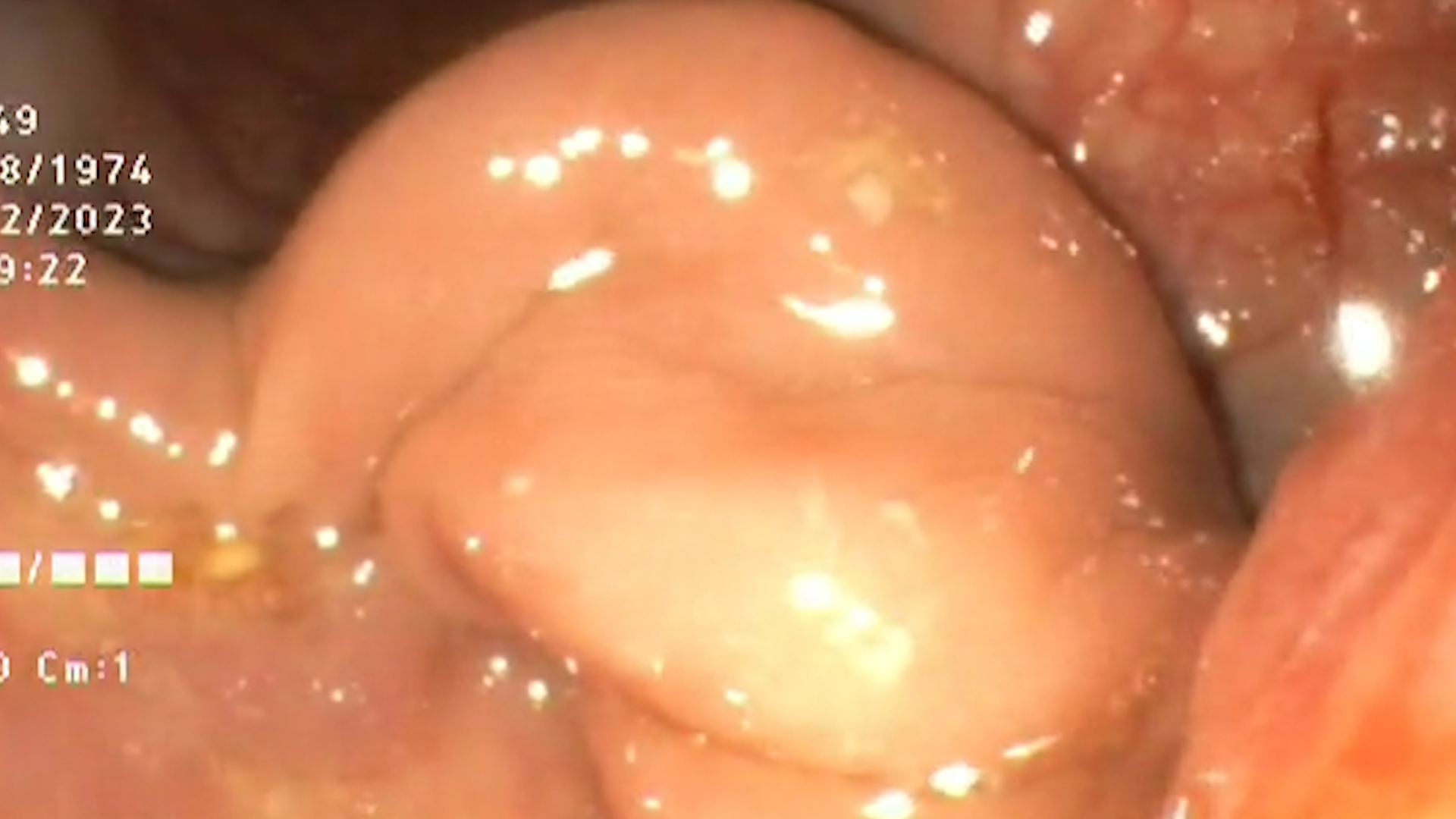
Ecoendoscopia a indicat o formațiune hipoecogenă dominantă (bine vascularizată) la nivelul corpului pancreatic, de aprox. 20 mm diametru (Figura 1-2), din care s-a efectuat puncție fina aspirativă bioptică ghidată (EUS-FNB) (Figura 3). Au fost evidențiate și multiple alte formațiuni hipoecogene (> 10) localizate la nivelul capului, corpului și cozii de pancreas, cu dimensiuni variabile de 3-5-7 mm, din care s-a efectuat puncție fină aspirativă bioptică ghidată (EUS-FNB) (Figura 4). Imagistica SPECT -CT cu Tc99m Tektrotyd a indicat pozitivtate pentru leziunea corporeală.
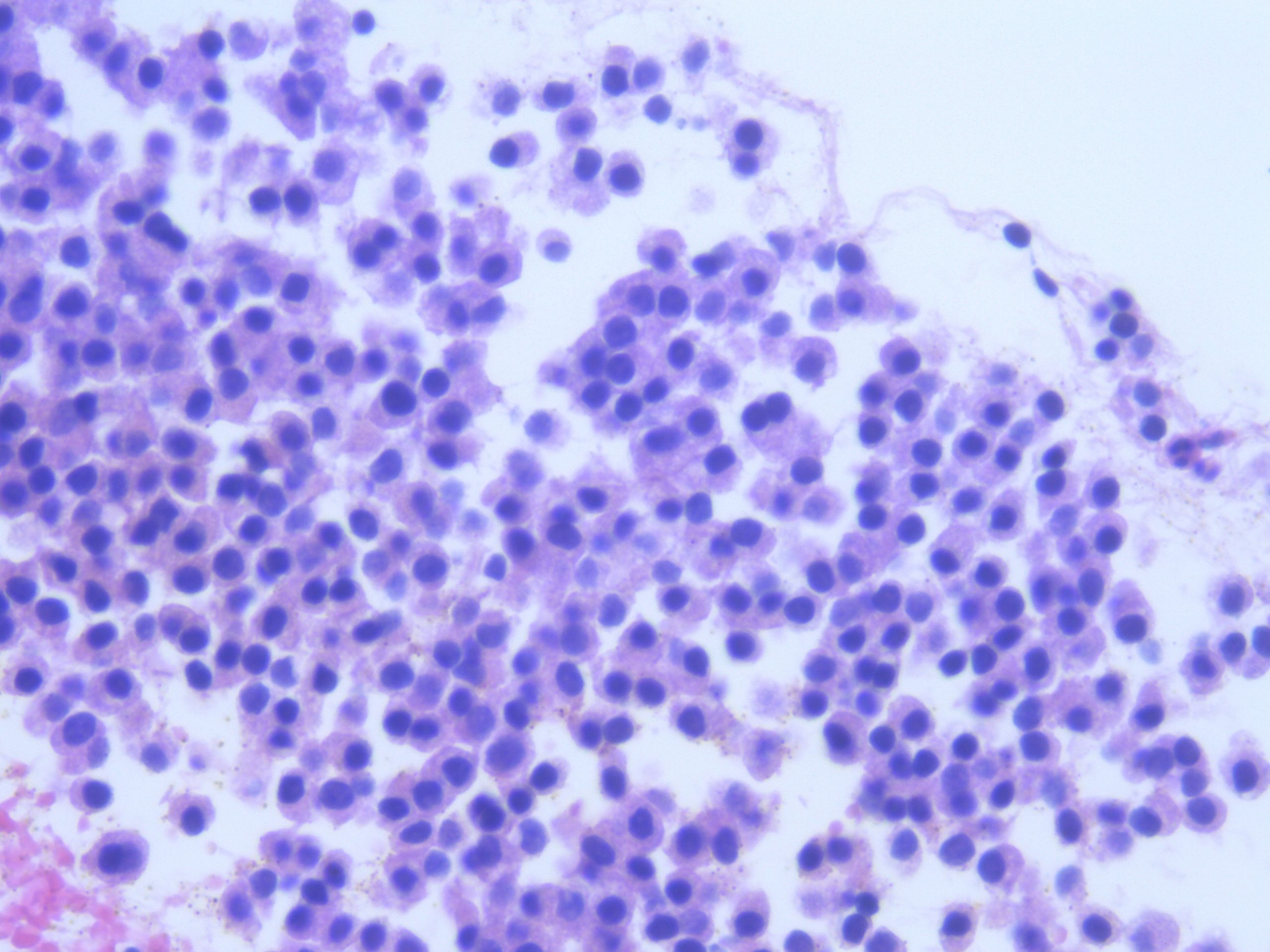
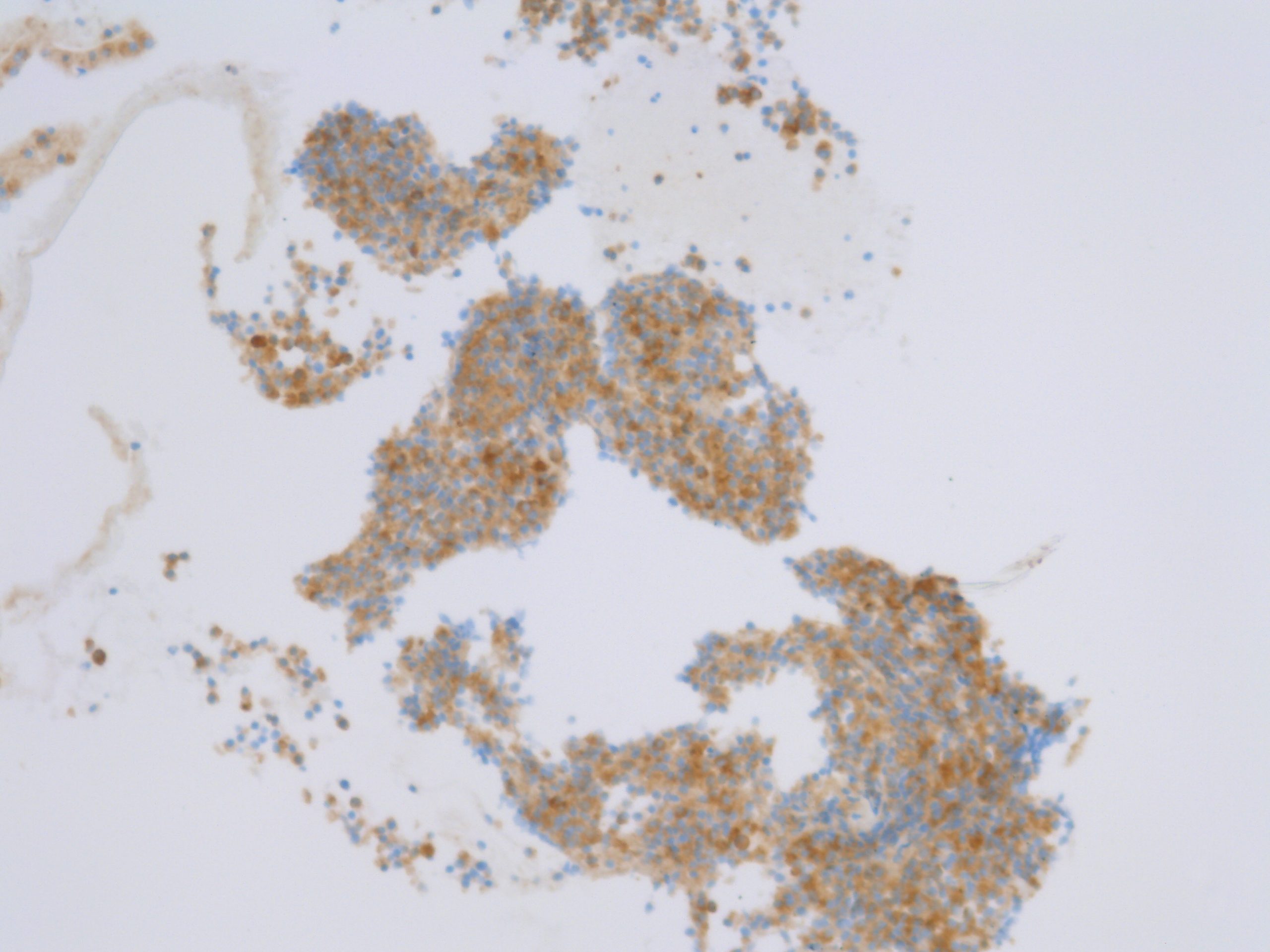
Puncția fină aspirativă bioptic cu ac fin de tip “histologic” s-a efectuat ghidat ecoendoscopic (EUS-FNB) în formațiunea dominantă corporeală și formațiunile tumorale diminutive caudale, confirmând diagnosticul de tumoră neuroendocrină bine diferențiată (Pan-NEN G1). A fost efectuat examen citologic (pe lamă) și microhistologic (prin prelucrare la parafină a blocului cellular), cu colorații convenționale hematoxilină-eozină (Figura 5) și respectiv imunohistochimice, cu pozitivitate pentru CK AE1/AE3 (difuz perinuclear), sinaptofizină (difuz) (Figura 6), cromogranină (focal) (Figura 7) și Ki67(2%). Au fost de asemenea evidențiați receptori SMS (pozitivitate SMS SSTR2 > 66% din celulele tumorale).
Gena MEN1 a fost analizată prin PCR și secvențiere bidirecțională a regiunii codificatoare + splicing pentru joncțiuni intron-exon. MLPA a fost, de asemenea, aplicat ștergerilor /dublărilor identificate. A fost identificată deleția heterozigotă a 80 de nucleotide de la intronul 6 la exonul 7 al genei MEN1 (c.928-33_963del) – mutație clasa 4 (posibil patogenă). Consecința biologică este reprezentată de pierderea situsului de splicing la nivelul intronului 6, precum și a 36 de nucleotide la porțiunea 5’ finală a exonului 7, cu un exon 7 lipsă din produsul proteic final. În concluzie, pacientul este afectat de MEN-1 ca o consecință a deleției menționate, cu prognostic relativ bun1.
Pacientul urmează tratament cu Pantoprazol (40 mg x 2/zi), Sandostatin LAR (20 mg x 2/lună) și Sutent (200 mg/zi), fiind candidat pentru tratament PRRT (peptide receptor radionucleotide therapy) cu LUTATHERA (Lu 177 DOTATATE)2. Tratamentul chirurgical a fost temporizat3.
Prezentarea ilustrează rolul ecoendoscopiei pentru evaluarea unei tumori neuroendocrine pancreatice rare (gastrinom SRS pozitiv), cu multiple determinări secundare intrapancreatice. Puncția fină aspirativă ghidată ecoendoscopic a permis stabilirea unui diagnostic de certitudine prin examen histopatologic cu colorații imunohistochimice.
1. van Beek DJ, Nell S, Pieterman CRC, et al . Prognostic factors and survival in MEN1 patients with gastrinomas: Results from the DutchMEN study group (DMSG). J Surg Oncol 2019; 120: 966-975.
2. Das S, Al-Toubah T, El-Haddad G, Strosberg J. 177Lu-DOTATATE for the treatment of gastroenteropancreatic neuroendocrine tumors. Expert Rev Gastroenterol Hepatol 2019; 13: 1023-1031.
3. Norton JA, Foster DS, Ito T, Jensen RT. Gastrinomas: Medical or Surgical Treatment. Endocrinol Metab Clin North Am 2018; 47: 577-601.