Vezi și alte cazuri
Pseudochist pancreatic drenat sub ghidaj ecoendoscopic
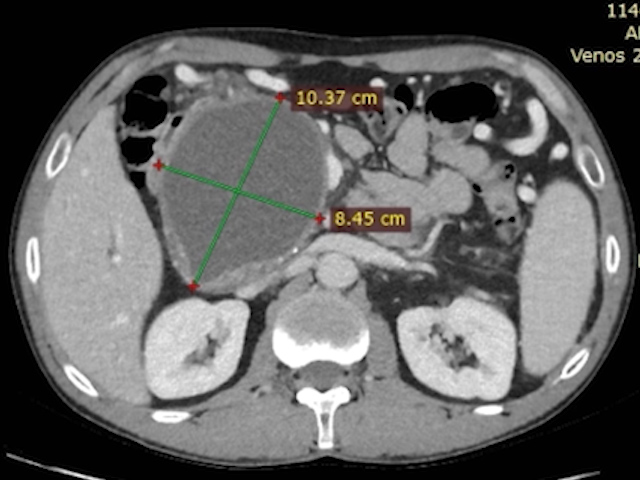
Bărbat de 45 de ani, cu antecedente de pancreatită acută, se prezintă la 6 luni după episod pentru evaluarea unui pseudochist cefalopancreatic. Aspectul imagistic computer tomografic (CT) arată un pseudochist de 50 × 45 mm, cu conținut clar și pereți subțiri.
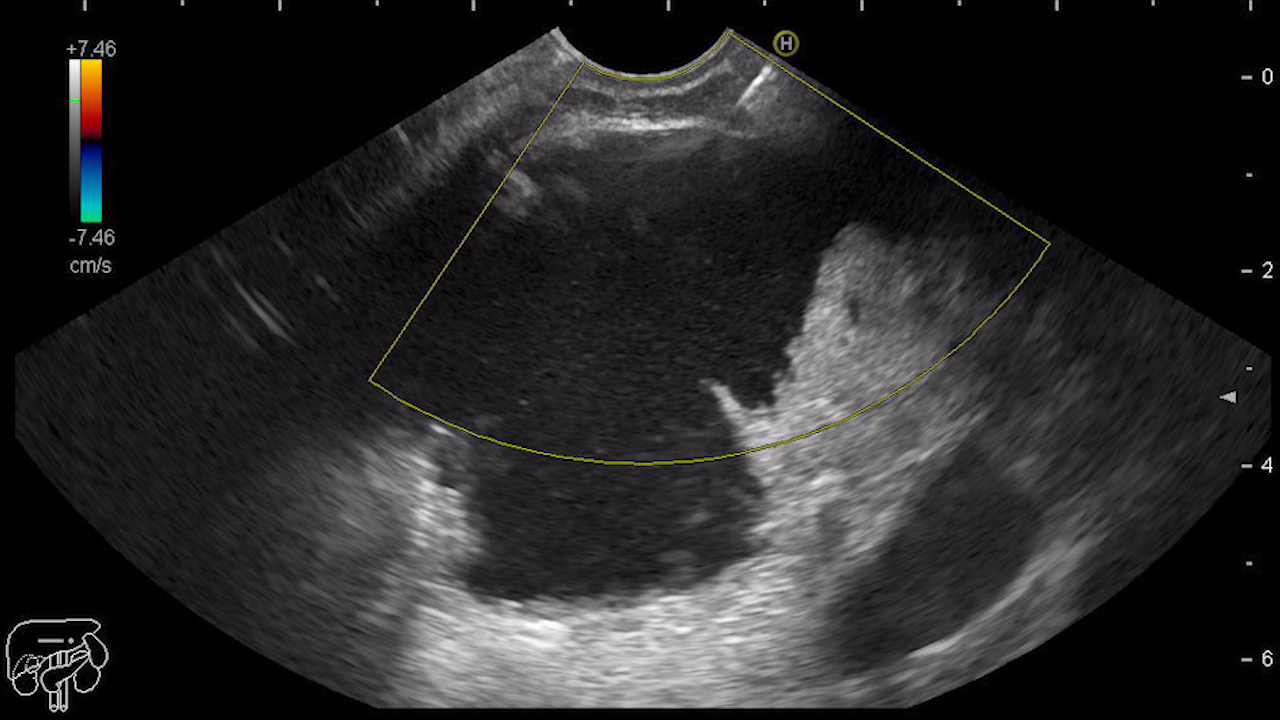
La internare, pseudochistul crescuse la 103 × 85 mm, cu efect compresiv asupra hilului hepatic (Fig.1). Pacientul acuza prurit generalizat și disconfort abdominal postprandial de aproximativ o lună. La examinare, prezenta sclere subicterice, abdomen suplu și dureros în etajul superior, fără semne de iritație peritoneală.
Biologic: sindrom de colestază (BT 3,4 mg/dL, BD 2,5 mg/dL, GGT 300 UI/L, fosfatază alcalină 320 UI/L); hemoleucograma și markerii de inflamație sunt în limite normale.
Ecoendoscopia (EUS) cu sondă liniară a fost efectuată pentru evaluarea oportunității drenajului și pentru excluderea altor cauze ale sindromului colestatic.
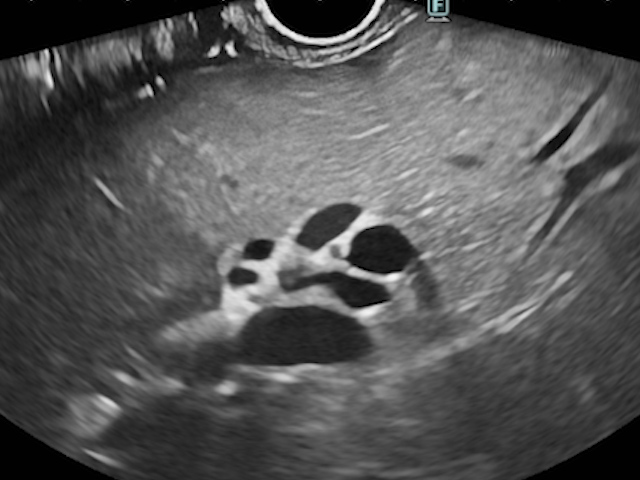
Pancreasul prezintă criterii de pancreatită cronică: duct pancreatic principal (DP) dilatat până la 7 mm, cu aspect moniliform și pereți ecogeni, dilatare de ducte secundare și calcificări intraparenchimatoase (Fig. 2). Strandurile ecogene delimitează lobuli hipoecogeni, iar ductele secundare prezintă dilatări segmentare.
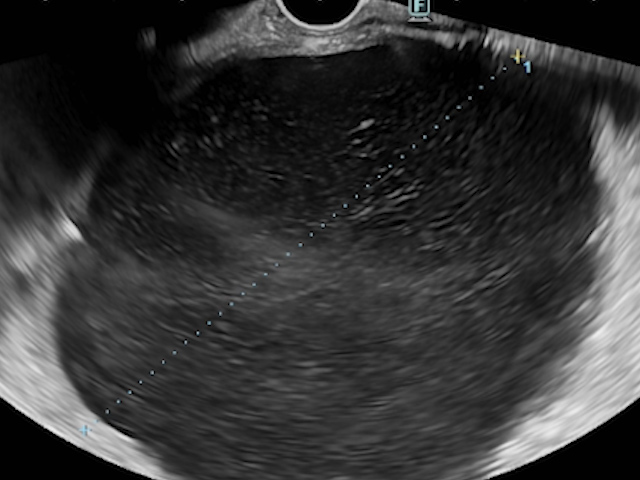
Pseudochistul cefalopancreatic măsoară 83,5 mm, fără componentă solidă, cu perete subțire de 2,7 mm. Vizibilitatea de la nivelul stației gastrice permite realizarea unei chistogastroanastomoze ghidate EUS (CGA-EUS). Ecoendoscopul se poziționează și în statia duodenală pentru urmărirea ductului pancreatic de la nivelul papilei, care pare doar comprimat, fără comunicare cu colecția fluidă pancreatica. Calea biliară principală (CBP) este dilatată până la 14,6 mm, iar căile biliare intrahepatice (CBIH) sunt dilatate în ambii lobi (Fig. 3).
Se stabilește diagnosticul de pancreatită cronică calcifiantă cu pseudochist cefalopancreatic cu efect obstructiv și sindrom de colestază.
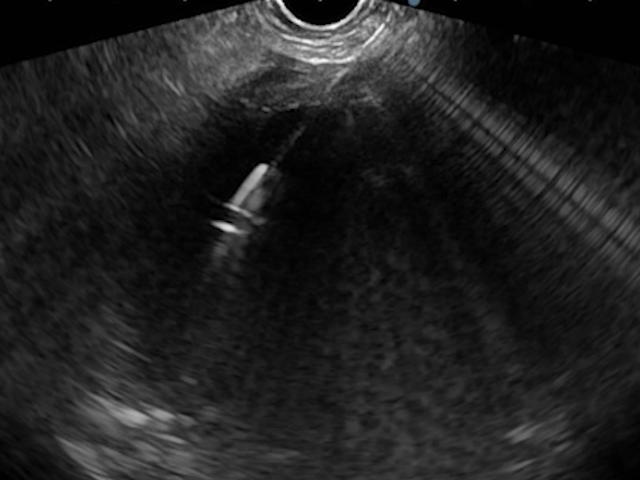
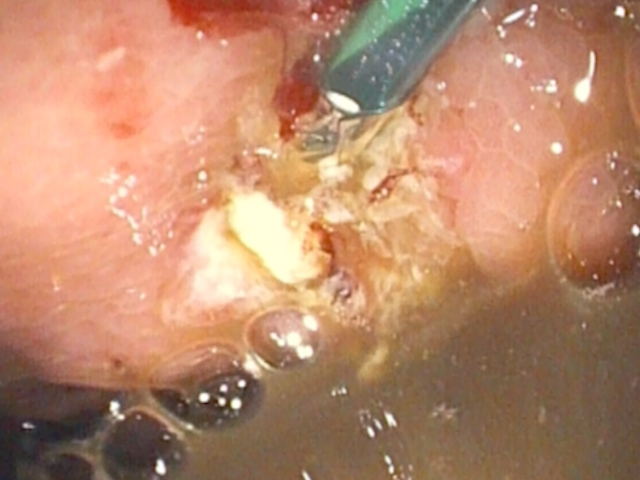
S-a efectuat CGA EUS cu stent plastic tip pigtail. Sub sedare profundă și intubare orotraheală, colecția a fost puncționată cu ac FNA de 19G, iar aspiratul, cu aspect ruginiu, a fost trimis pentru analize biologice și bacteriologice (Fig. 4).
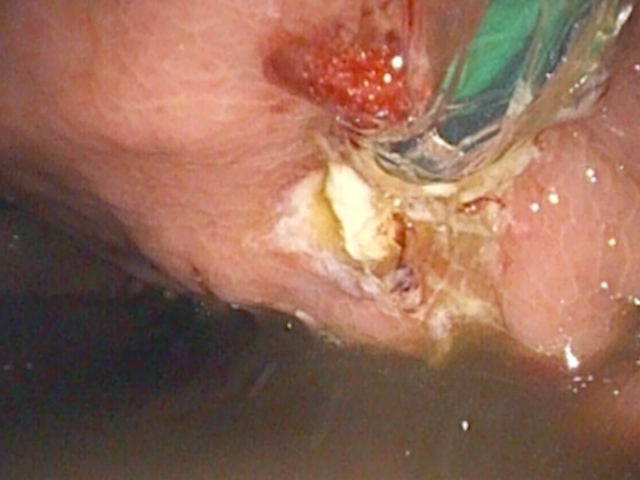
Firul ghid de 0,0035 inch a fost introdus și buclat de două ori în colecție sub ghidaj fluoroscopic. Pe firul ghid s-a realizat cistotomie cu dispozitiv de 10G (Cook), perforând atât peretele gastric, cât și cel al colecției (Autocut 110 W) (Fig. 5).
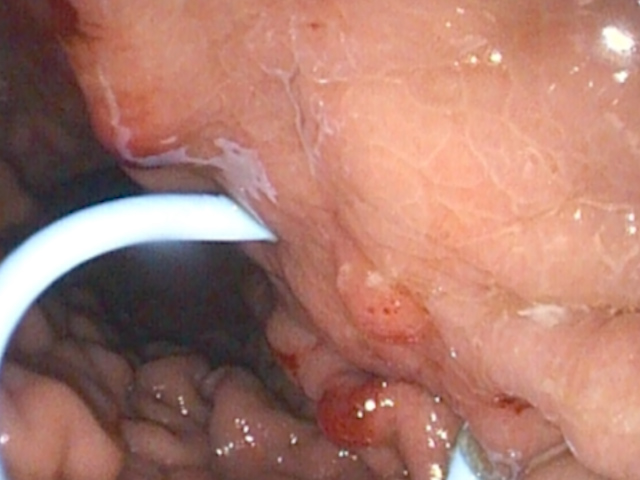
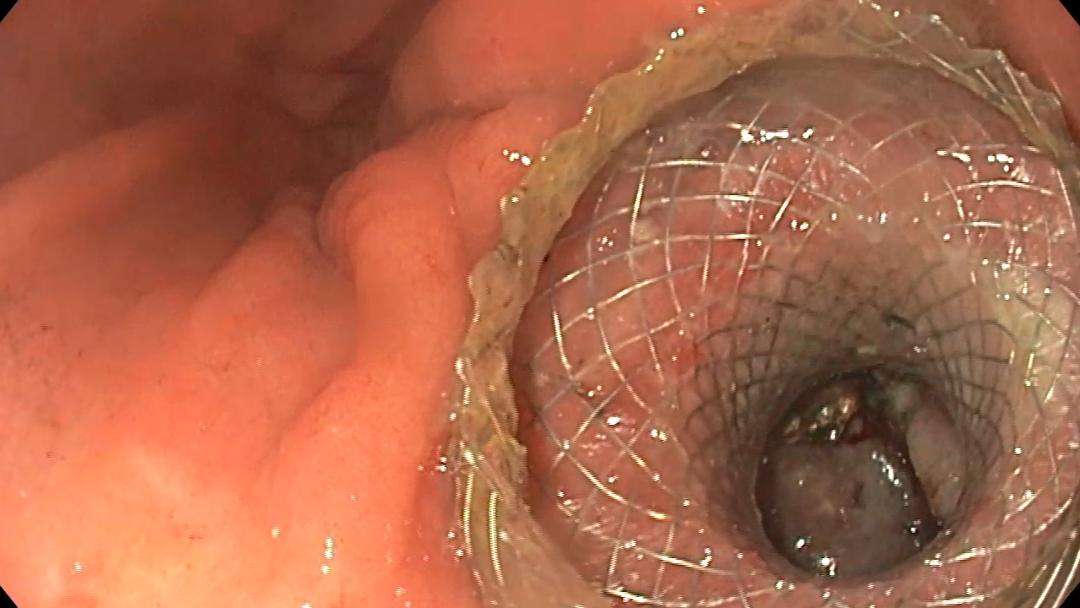
Tractul a fost dilatat cu balon de 8 mm (Fig. 6), iar procedura s-a încheiat cu montarea unui stent biliar pigtail de 10 Fr / 5 cm (Fig. 7). Procedura s-a desfășurat fără incidente, iar pacientul a revenit pe secția de gastroenterologie la 4 h după detubare.
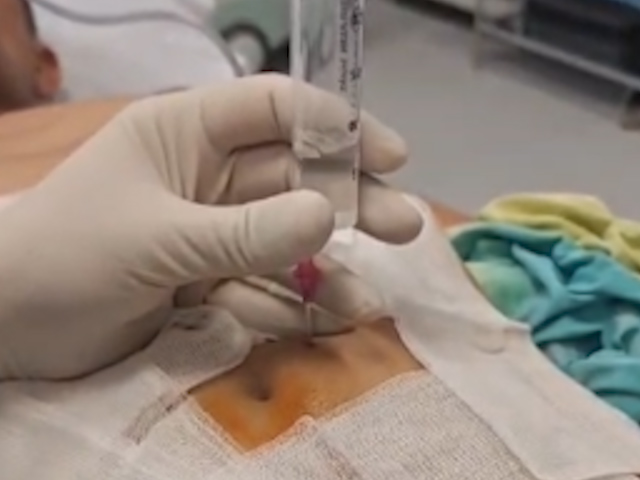
În primele 24 h, pruritul s-a remis, iar probele de colestază s-au normalizat; pacientul acuza ușor disconfort abdominal. S-a identificat pneumoperitoneu minor, gestionat conservator prin drenaj percutan simplu (Fig. 8). Pacientul a fost externat asimptomatic la 48 h, iar la controlul de 30 zile pseudochistul regresase semnificativ (27 mm), cu stentul biliar în situ.
Complicațiile locale ale pancreatitei acute ce pot apărea la 4-6 săptămâni includ colectii necrotice sau walled-off necrosis (WON) și colectii fluide pancreatice sau pseudochist pancreatic [1].
Drenajul ghidat prin EUS este metoda preferată pentru PFC, înlocuind abordările chirurgicale sau radiologice intervenționale, cu succes clinic similar, dar morbiditate și costuri reduse [2]. Drenajul se realizează cu stenturi de plastic tip pigtail (SPP) sau stenturi metalice de apozitie a lumenelor (LAMS). LAMS sunt recomandate în tratamentul WON, SPP pentru drenajul pseudochisturilor pancreatice [3-5]. Se pot plasa mai multe stenturi sau ghiduri simultan; eficiența unui singur SPP este de 94% [6]. Stenturile multiple mențin fistula, permit drenaj prin și între stenturi și reduc riscul de migrare, cu rată de succes 83-100% [7,8]. Stenturile mici (ex. 7 Fr) au rate mai mari de obstrucție; diametre mai mari sunt preferate, deși utilizarea stenturilor de 7 Fr nu este incorectă [2]. Fluoroscopia optimizează vizualizarea, accesul și poziția dispozitivelor, dar nu este obligatorie. Studiul prospectiv Seicean et al. a utilizat SPP fără fluoroscopie, cu succes tehnic în 83,3% (20/24), toate eșecurile fiind la PFC <6 cm și pereți >2 mm [9].
Cele mai frecvente complicații ale cistogastrostomiei ghidate EUS includ hemoragie, infecție, perforație, migrarea sau obstrucția stentului, pneumoperitoneu, sângerare tardivă din pseudoanevrisme și persistența fistulei gastrice [10,11]. Pneumoperitoneul fără peritonită, o complicație rară (<5%), apare de obicei prin scăpare tranzitorie de aer în peritoneu în timpul dilatării tractului de drenaj sau prin pasaj minor de aer prin canalul fistulos în perioada postprocedurală. În absența lichidului peritoneal și a semnelor clinice de peritonită, se poate adopta observație clinică și, la nevoie, drenaj percutan simplu [12].
Cazul demonstrează eficiența drenajului EUS-ghidat al unui pseudochist cefalopancreatic cu stent plastic, siguranța managementului conservator al pneumoperitoneului minor și importanța selecției tipului de stent conform caracterului colecției și ghidurilor ESGE.
- Banks PA, Bollen TL, Dervenis C, Gooszen HG, Johnson CD, Sarr MG, Tsiotos GG, Vege SS; Acute Pancreatitis Classification Working Group. Classification of acute pancreatitis–2012: revision of the Atlanta classification and definitions by international consensus. Gut. 2013 Jan;62(1):102-11. doi: 10.1136/gutjnl-2012-302779. Epub 2012 Oct 25. PMID: 23100216.
- Teoh AY, Dhir V, Jin ZD, Kida M, Seo DW, Ho KY. Systematic review comparing endoscopic, percutaneous and surgical pancreatic pseudocyst drainage. World J Gastrointest Endosc. 2016 Mar 25;8(6):310-8. doi: 10.4253/wjge.v8.i6.310. PMID: 27014427; PMCID: PMC4804189.
- Dumonceau JM, Delhaye M, Tringali A, Arvanitakis M, Sanchez-Yague A, Vaysse T, Aithal GP, Anderloni A, Bruno M, Cantú P, Devière J, Domínguez-Muñoz JE, Lekkerkerker S, Poley JW, Ramchandani M, Reddy N, van Hooft JE. Endoscopic treatment of chronic pancreatitis: European Society of Gastrointestinal Endoscopy (ESGE) Guideline – Updated August 2018. Endoscopy. 2019 Feb;51(2):179-193. doi: 10.1055/a-0822-0832. Epub 2019 Jan 17. PMID: 30654394.
- van der Merwe SW, van Wanrooij RLJ, Bronswijk M, Everett S, Lakhtakia S, Rimbas M, Hucl T, Kunda R, Badaoui A, Law R, Arcidiacono PG, Larghi A, Giovannini M, Khashab MA, Binmoeller KF, Barthet M, Perez-Miranda M, van Hooft JE. Therapeutic endoscopic ultrasound: European Society of Gastrointestinal Endoscopy (ESGE) Guideline. Endoscopy. 2022 Feb;54(2):185-205. doi: 10.1055/a-1717-1391. Epub 2021 Dec 22. PMID: 34937098.
- van Wanrooij RLJ, Bronswijk M, Kunda R, Everett SM, Lakhtakia S, Rimbas M, Hucl T, Badaoui A, Law R, Arcidiacono PG, Larghi A, Giovannini M, Khashab MA, Binmoeller KF, Barthet M, Pérez-Miranda M, van Hooft JE, van der Merwe SW. Therapeutic endoscopic ultrasound: European Society of Gastrointestinal Endoscopy (ESGE) Technical Review. Endoscopy. 2022 Mar;54(3):310-332. doi: 10.1055/a-1738-6780. Epub 2022 Feb 3. PMID: 35114696.
- Lin H, Zhan XB, Sun SY, Yang XJ, Jin ZD, Zou DW, Li ZS. Stent selection for endoscopic ultrasound-guided drainage of pancreatic fluid collections: a multicenter study in china. Gastroenterol Res Pract. 2014;2014:193562. doi: 10.1155/2014/193562. Epub 2014 Jun 11. PMID: 25018767; PMCID: PMC4074944.
- Giovannini M, Bernardini D, Seitz JF. Cystogastrotomy entirely performed under endosonography guidance for pancreatic pseudocyst: results in six patients. Gastrointest Endosc. 1998 Aug;48(2):200-3. doi: 10.1016/s0016-5107(98)70165-8. PMID: 9717789.
- Seifert H, Dietrich C, Schmitt T, Caspary W, Wehrmann T. Endoscopic ultrasound-guided one-step transmural drainage of cystic abdominal lesions with a large-channel echo endoscope. Endoscopy. 2000 Mar;32(3):255-9. doi: 10.1055/s-2000-93. PMID: 10718392.
- Seicean A, Stan-Iuga R, Badea R, Tantau M, Mocan T, Seicean R, Iancu C, Pascu O. The safety of endoscopic ultrasonography-guided drainage of pancreatic fluid collections without fluoroscopic control: a single tertiary center experience. J Gastrointestin Liver Dis. 2011 Mar;20(1):39-45. PMID: 21451796.
- Puri R, Thandassery RB, Alfadda AA, Kaabi SA. Endoscopic ultrasound guided drainage of pancreatic fluid collections: Assessment of the procedure, technical details and review of the literature. World J Gastrointest Endosc. 2015 Apr 16;7(4):354-63. doi: 10.4253/wjge.v7.i4.354. PMID: 25901214; PMCID: PMC4400624.
- Kinoshita K, Okamoto K, Noguchi H, Fukuchi S, Akiyama H, Motomura M, Azuma Y, Hiroshima Y, Fuchino T, Ozaka S, Sagami R, Uchida T, Hirashita Y, Fukuda K, Ogawa R, Mizukami K, Kodama M, Murakami K. Efficacy of Endoscopic Ultrasound-guided Transluminal Drainage Using Lumen-apposing Metal Stents for the Treatment of Pancreatic Fluid Collections. DEN Open. 2025 Nov 22;6(1):e70249. doi: 10.1002/deo2.70249. PMID: 41287748; PMCID: PMC12640457.
- Prochazka Zárate R, Vidales Mostajo G, Villa-Gómez Roig G, Illescas Castellanos A, Pereira Robles N. Neumoperitoneo a tensión como complicación de drenaje transgástrico de pseudoquiste pancreático guiado por ultrasonografía endoscópica. Reporte de caso clínico y revisión de la literatura [Tension pneumoperitoneum as a complication of endoscopic ultrasound guided transgastric drainage of pancreatic pseudocyst: case report and review of the literature]. Rev Gastroenterol Peru. 2012 Jan-Mar;32(1):88-93. Spanish. PMID: 22476184.